Modelling the S-Doped Sodalites Using DFT, TD-DFT and SAC-CI Methods
A. Curutchet and T. Le Bahers, Inorg. Chem. 2017, 56, 414-423
Il s’agit de ma première publication sur le sujet des minéraux ténébrescents. Ce travail uniquement fondé sur la chimie quantique a pour objectif de démontrer que cet outil peut être utilisé pour modéliser le photochromisme des sodalites.
Nous avons entre autres montré que pour modéliser l’absorption du centre F par une approche type cluster, une cage-β entière doit être considérée dans le cluster traité au niveau quantique et que le couplage vibronique doit être inclus. La transition électronique de l’électron piégé couple fortement avec le mode de vibration correspondant à la respiration du tétraèdre de sodium.
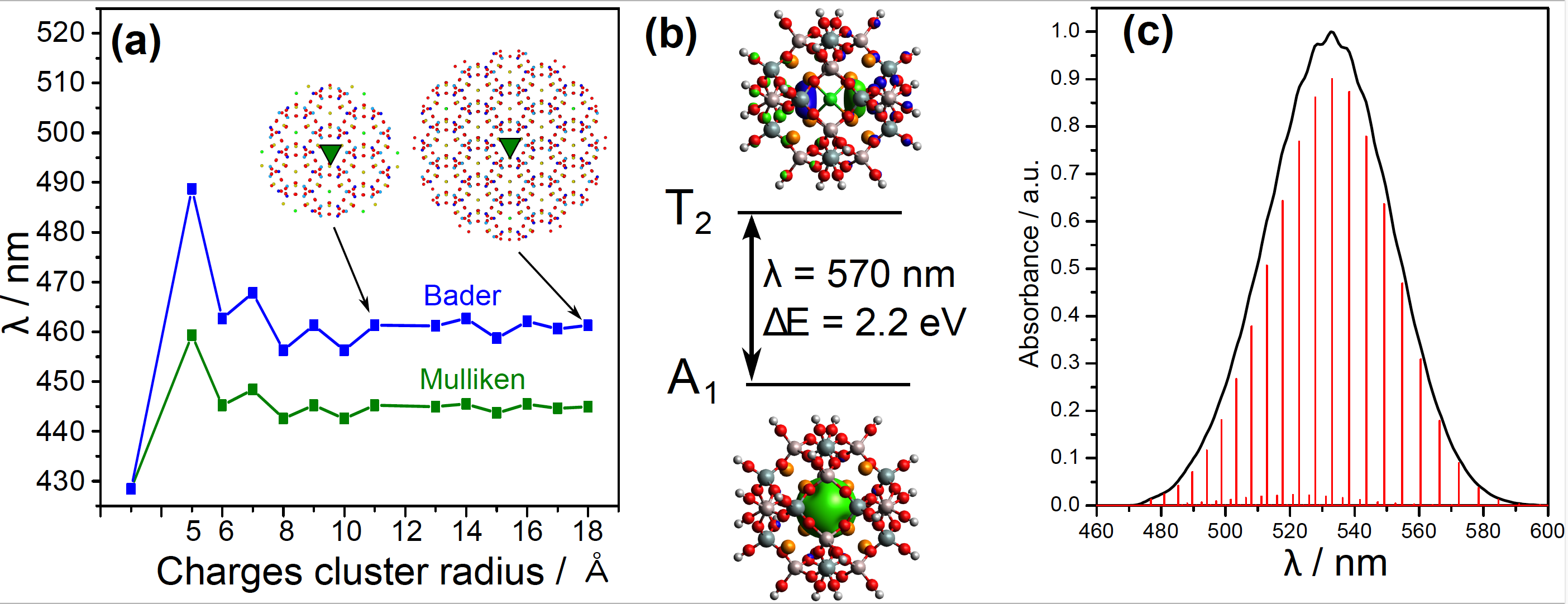
Figure 1: (a) Longueur d'onde d'absorption du système [Na4VCl]3+ entouré par un cluster de charges ponctuelles (charges Mulliken ou Bader) de taille croissante. A l'intérieur, le triangle vert est la partie QM et les points sont les positions des charges. (b) Longueur d'onde d'absorption calculée en TD-DFT pour le cluster incluant la cage-β, sans charges ponctuelles. (c) Spectre d'absorption simulé incluant le couplage vibronique, avec uniquement les vibrations du tétraèdre Na4 .
Nous avons montré que le transfert de charge depuis l’impureté S22- vers la lacune de chlore est responsable de la formation du centre-F avec des énergies de transition en accord avec l’expérience.
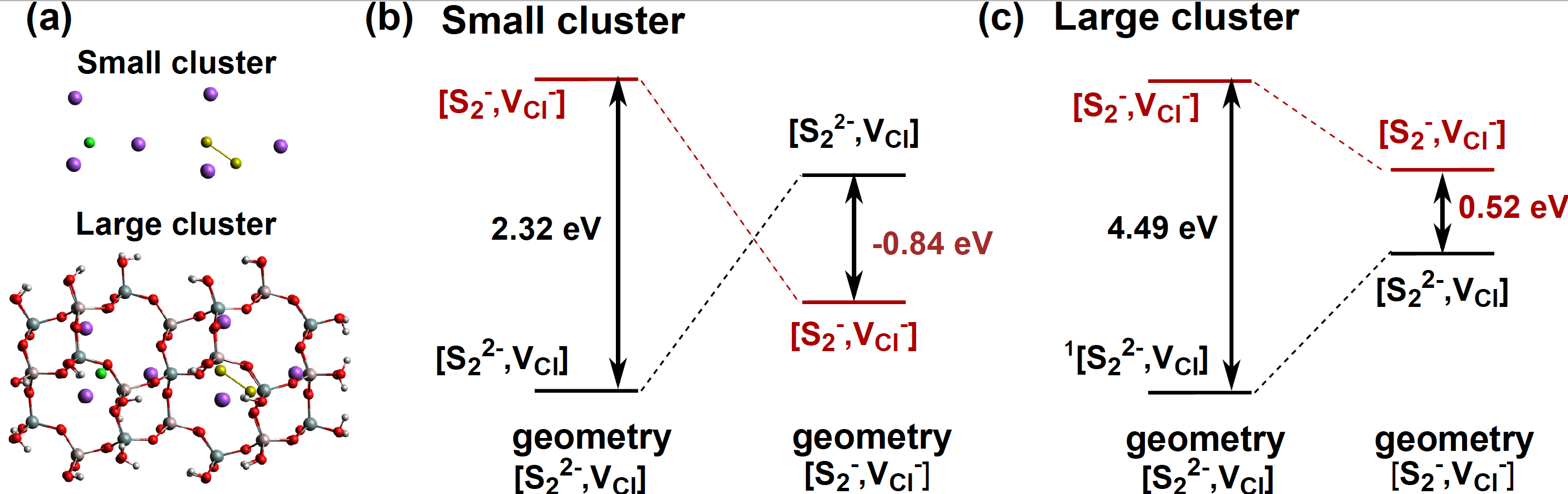
Figure 2: (a) Structures du petit et du grand cluster. (b) et (c) Energies de transition calculées par SAC-CI pour les deux clusters.
Solar UV Index and UV Dose Determination with Photochromic Hackmanites: From the Assessment of Fundamental Properties to the Device
I. Norrbo, A. Curutchet, A. Kuusisto, J. Mäkelä, P. Laukannen, P. Paturi, T. Laihinen, J. Sinkkonen, E. Wetterskog, F. Mamedov, T. Le Bahers, M. Lastusaari, Mater. Horiz. 2018, 5, 569-576
Cet article est le premier de la collaboration avec le groupe de Mika Lastusaari. Dans cette étude, nous prouvons de manière expérimentale et théorique que la substitution partielle des sodiums par un autre alcalin (K ou Rb) conduit à une diminution de l’énergie de la transition à transfert de charge de S22 vers la lacune de chlore.
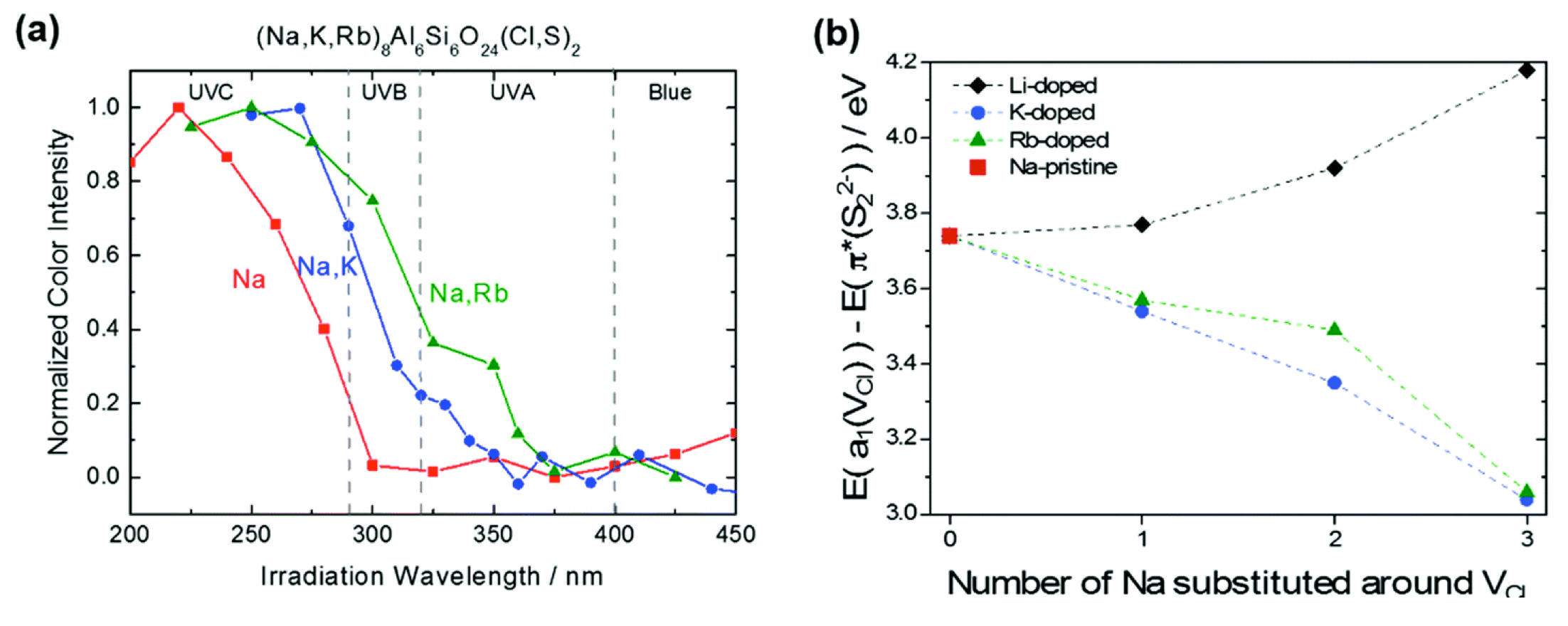
Figure 3: (a) Spectres d'excitation de ténébrescence de (Na,M)8Al6Si6O24(Cl,S)2 (M = aucun, K et Rb) avec 6% de dopage S. (b) Variation du gap calculée au niveau DFT (en eV) entre la dernière orbitale occupée π*(S22−) et la première orbitale vacante a1(VCl) en fonction du nombre de Na substitué autour de la lacune de Cl.
De plus, dans ce travail, le groupe de Mika Lastusaari présente pour la première fois l’expérience de thermoténébrescence permettant de mesurer l’énergie d’activation du blanchiment de la sodalite. Cette énergie d’activation mesurée (environ 0.4 eV) s’est trouvée en bon accord avec la valeur théorique proposé dans étude purement théorique publiée précédemment dans Inorganic Chemistry.
Enfin, nous proposons d’utiliser les hackmanites ténébrescentes artificielles comme indicateur IV car la sensibilité de ces matériaux aux UV peut être adaptée pour des UV spécifiques (tel que les UV provenant du soleil).
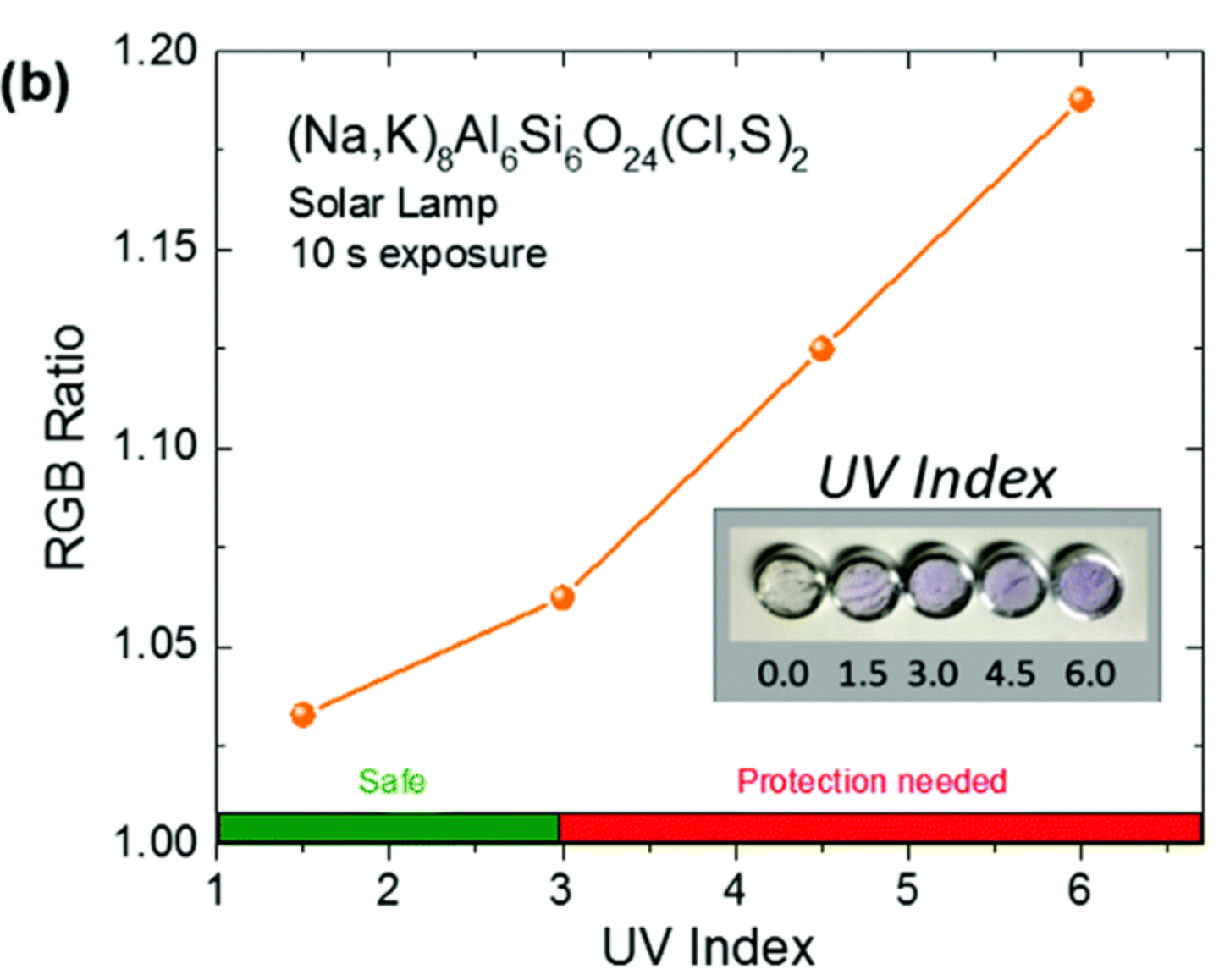
Figure 4: Intensité de couleur de (Na,K)8Al6Si6O24(Cl,S)2 pour différentes valeurs d'indice UV.
On the Spectrosocpic Modelling of Localized Defects in Sodalites by TD-DFT
P. Colinet, A. Gheeraert, A. Curutchet, T. Le Bahers, J. Phys. Chem. C, 2020, 124, 8949-8957.
Dans cette étude, nous avons amélioré l'approche cluster introduite dans notre premier article sur la ténébrescence des sodalites. Ce travail a porté sur la simulation des propriétés spectroscopiques de deux défauts ponctuels à savoir un électron piégé et les anions dichalcogènures.
Figure 5 : Orbitales impliquées dans l'absorption de l'électron piégé (à gauche) présentant une déliocalisaiton sur la cage aluminosilicate. Orbitales impliquées dans le spectre d'émission de l'ion S2- (à droite) ne présentant pas de délocalisation sur la cage aluminosilicate.
Figure 6 : Spectre d'absorption du centre coloré (à gauche) et d'émission de l'ion S2- (à droite) simulés pour différent types d'environnement au niveau TD-PBE0. La courbe bleue est obtenue par la prise en compte du couplage vibronique.
La principale conclusion porte sur l'influence de l'environnement sur la simulation des propriétés spectroscopiques. Bien qu'un électron piégé et l'ion S2- soient tous les deux défauts ponctuels, ils n'ont pas la même sensibilité à l’environnement utilisé lors du calcul des états excités (Figure 6). Une analyse rapide de la délocalisation des orbitales (comme sur la Figure 5) permet de se faire une idée sur le rôle que jouera l'environnement sur le résultat du calcul.
Hackmanite - The Natural Glow in the Dark Mineral
C. Agamah, S. Vuori, P. Colinet, I. Norrbo, J. Miranda de Cavalho, N. K. O. Nakamura, J. Lindblom, L. van Goethem, A. Emmermann, T. Saarinen, T. Laihinen, E. Laakkonen, J. Lindén, K. Konu, H. Vrielinck, D. Van der Haagen, P. F. Smet, T. Le Bahers, M. Lastusaari, Chem. Mater. 2020, 32, 8895-8905.
Cet article porte sur un autre phénomène spectroscopique observé dans les hackmanites, la luminescence persistante. Nous avons montré que cette luminescence persistante était due à la présence d'ions Ti3+ qui par excitation lumineuse permettant le transfert d'un électron du Ti3+ vers une lacune d'oxygène. C'est le retour activé thermiquement de cet électron vers le titane qui est responsable de la luminescence. Nous avons aussi montré qu'il y avait une compétition entre le phénomène de luminescence persistante et le photochromisme. Les zones où le photochromisme étaient observés ne donnaient jamais de luminescence persistante. En combinant des calculs par DFT et TD-DFT à l'expérience, nous avons émis l'hypothèse que les photons émis par luminescence persistante étaient absorbés par la transition à transfert de charge caractéristique du photochromisme.
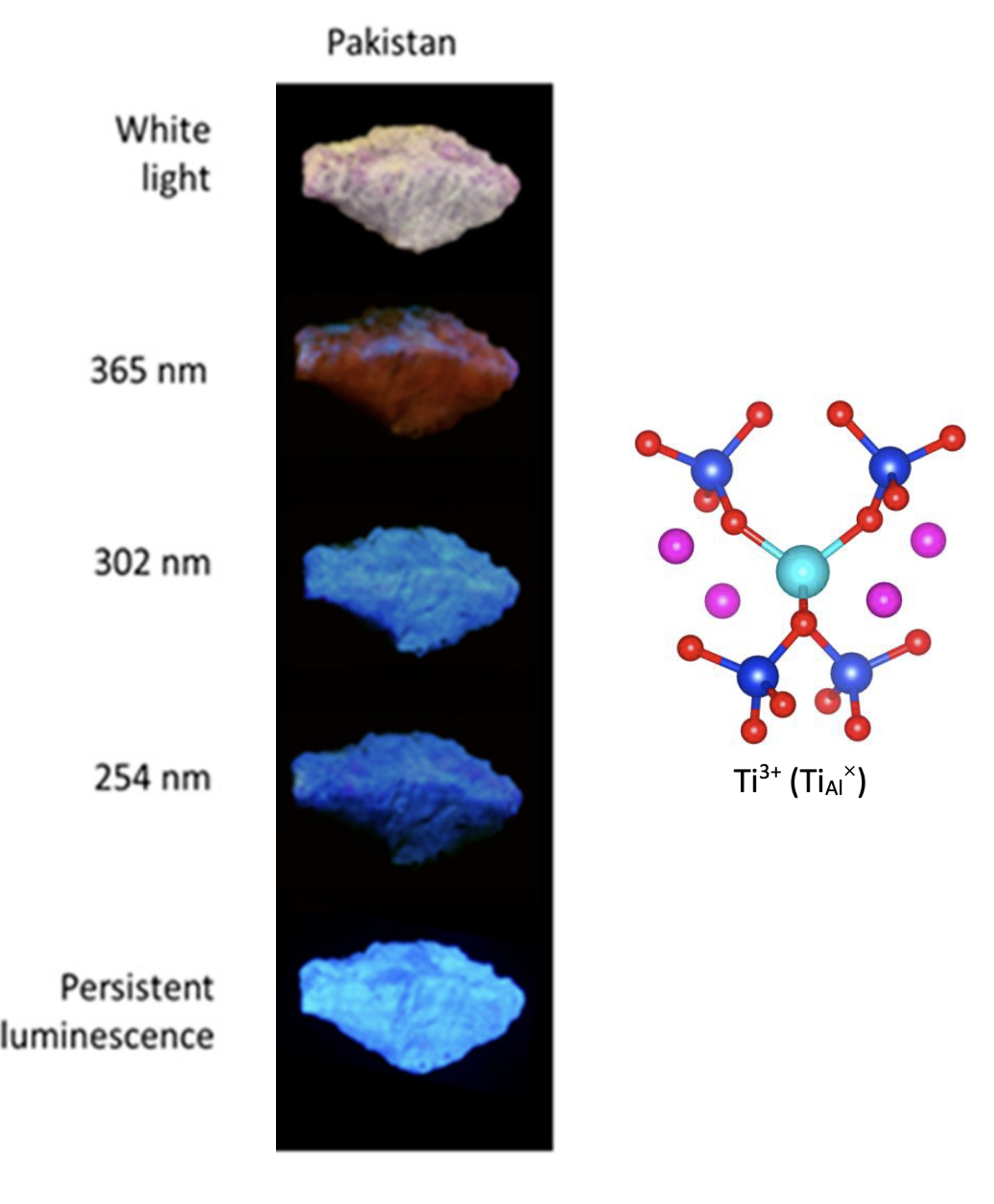
Figure 7 : Photo de l’émission d'une hackmanite en fonction de la longueur d'onde d'excitation (à gauche). Cluster utilisé pour simuler les propriétés spectroscopiques du Ti3+ (à droite).
Detection of X-ray Doses with Color-Changing Hackmanites: Mechanism and Application
S. Vuori, P. Colinet, I. Norrbo, R. Steininger, T. Saarinen, H. Palonen, P. Paturi, L. C. V. Rodrigues, J. Göttlincher, T. Le Bahers, M. Lastusaari, Adv. Opt. Mater., 2021, 9, 2100762.
Dans cet étude, nous montrer que le photochromisme peut aussi être observé par exposition des hackmanites aux rayons X. Mais le mécanismes est différent d'une activation UV. Dans le cas des rayons X, ce n'est pas une transition à transfert de charge qui est responsable de la formation d'un centre coloré, mais un mécanisme de scintillation. Les rayons X génèrent un grand nombre d'électrons et trous "chauds" dans le matériaux qui se thermalisent. Les électrons excités finissent par peupler la lacune de chlore donnant le centre colorant.
Nous avons montré qu'il était possible d'utiliser un film d'hackmanite comme détecteur de rayon X voire comme technique d'imagerie (cf Figure 8).
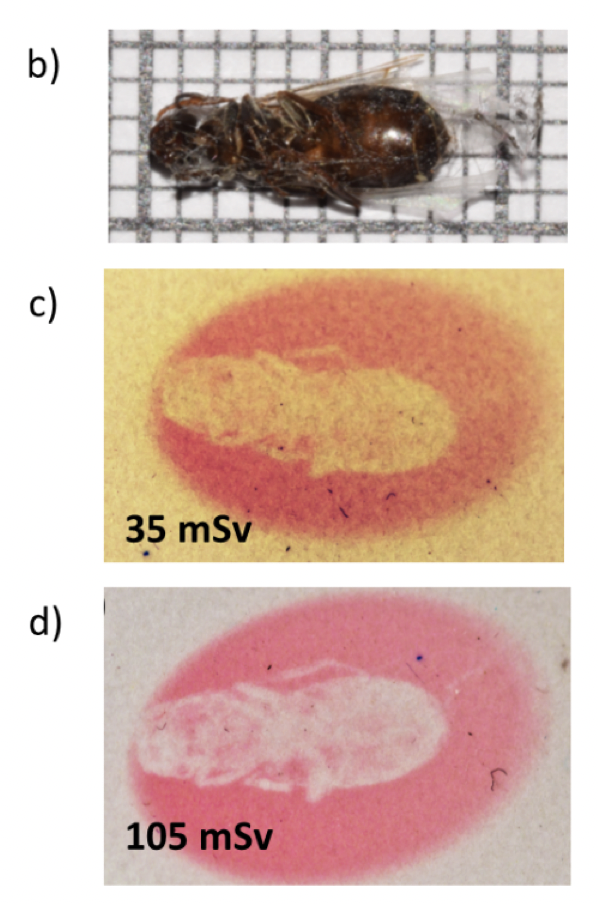
Figure 8 : Photo d'une mouche soumise à différente dose de rayons X.


